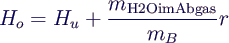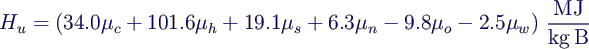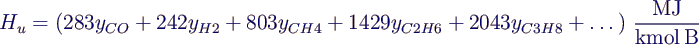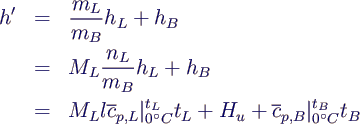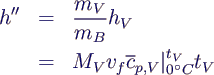Verbrennungsenthalpie
- Freiwerdende Energie bei Verbrennung:
- vollständige Verbrennung angenommen
- spezifisch (bezogen auf Masse des Brennstoffs)
- abhängig von
- Brennstoff
- Temperaturen von Brennstoff, Zuluft und
Verbrennungsgas
- Zustand der Verbrennungsprodukte (z.B. gasförmig
oder flüssig)
- Prozessführung (isobar oder isochor)
- durch verschiedene Normen beschrieben
- Heizwert und Brennwert:
-
Heizwert Hu (nach DIN 5499)
- bei t0 = 25 °C für Brennstoff,
Brennluft und Abgas
- Wasser dampfförmig
- CO2 und SO2 gasförmig
- keine Stickoxide
-
Brennwert Ho
- wie Heizwert, aber Wasser flüssig
- Zusammenhang
- Werte tabelliert
- Näherungsformel für feste und flüssige Brennstoffe
- Näherungsformel für gasförmige Brennstoffe
- Abhängigkeit von der Temperatur:
- Temperaturen tL und tV von
Luft und Abgas
- Temperatur tB des Brennstoffs
- damit auf mB bezogene Enthalpie h' vor
Verbrennung
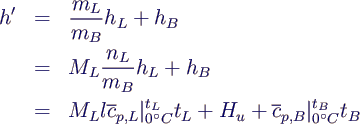
- (Bezugspunkt: hL = hB = 0
bei 0 °C)
- Enthalpie h'' nach der Verbrennung
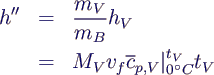
- (Bezugspunkt: hV = 0 bei 0 °C)
- Freiwerdende Wärme:
- Wärme pro Brennstoffmasse aus Enthalpiedifferenz
- wenn tV kleiner als Taupunkt →
- Wasser kondensiert
- zusätzliche Verdampfungsenthalpie r wird
frei
-
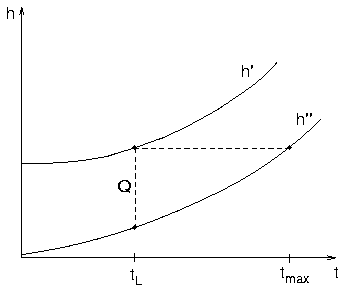
Adiabate Verbrennungstemperatur
tmax:
- keine Wärmeabfuhr → maximale Temperatur des
Verbrennungsgases
- tmax ergibt sich aus Enthalpiebilanz
- im Bild durch waagerechte Linie
- genauer: Dissipation der Moleküle berücksichtigen
- Aufgaben: