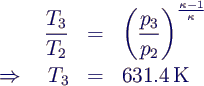Lösung von Aufgabe 1
- Bestimmen der Gasgrößen
- Zunächst gilt wegen der Isothermen:
- Die Adiabate 2 → 3 liefert
- Mit Hilfe der Beziehungen aus dem Abschnitt
Carnot-Prozess
erhält man die aufgenommene Wärme
- Q12 = -WV12 = -
p1 V1 ln (p2/p1)
- Das fehlende V1 folgt aus der
Gasgleichung zu
- V1 = m Ri
T1/p1 = 1.435 m3
- Damit
- Daraus erhält man die abgegebene Wärme
- Q34 = -WV34 = -
Q12 T3 / T1 = - 1256 kJ
- somit Nutzarbeit und Wirkungsgrad
- Wk = - (Q12 +
Q34) = -733.3 kJ
- η = -Wk/Q12 =
0.3686
- Entropieänderungen bei Isentropen = 0. Bei
Isothermen:
- S2 - S1 =
Q12/T1 = 1.989 kJ/K
- S4 - S3 =
Q34/T4 = -1.989 kJ/K
- Die Gesamtentropie des Gases ändert sich nicht.
- Entropieänderung der Wärmebäder:
- bei A abgegebene Wärme Q12 bei Temperatur
T1 →
- ΔSA = - 1989 kJ / 1000 K =
-1.989 kJ/K
- bei C aufgenommene Wärme Q34 bei
Temperatur T3 →
- ΔSC = 1256 kJ / 631.4 K = 1.989
kJ/K
- Entropie des Gesamtsystems aus Wärmebädern und Gas
hat sich nicht geändert (reversibler Vorgang).