Aggregatzustände
- Beobachtung:
- qualitativ verschiedene Stoffeigenschaften bei
bestimmten Bereichen von Druck und Temperatur
- Beispiel Wasser bei Normaldruck: Wechsel bei 0 °C
und 100 °C
- Aggregatzustände fest, flüssig, gasförmig
- verschiedene Aggregatzustände können koexistieren
(mehrere Phasen)
- Beispiele:
- Eis und Wasser bei Normaldruck und 0 °C
- Wasser und Wasserdampf bei Normaldruck und 100
°C
- Stoffeigenschaften oft für verschiedene Phasen sehr
unterschiedlich, z.B. bei Wasser
-
| T [°C] |
Phase |
cp [kJ/(kg K)] |
| 0 |
fest |
1.93 |
| 0 |
flüssig |
4.22 |
| 100 |
flüssig |
4.19 |
| 100 |
gasförmig |
2.03 |
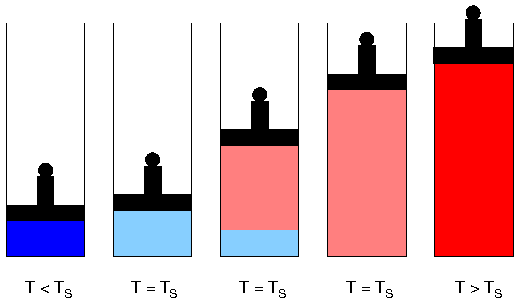
- Verdampfen:
- Übergang von der flüssigen in die gasförmige
Phase
- bei konstantem Druck:
- Siedetemperatur hängt vom Druck ab
- Zustand bei Siedetemperatur und gegebenem Druck
- verschiedenes Volumen möglich → nicht
eindeutig bestimmt
- zwei Phasen (Wasser und Dampf)
- weitere Zustandsgröße x (Dampfgehalt) zur
Beschreibung
- x = mGas / (mGas +
mFlüssigkeit)
- Technische Bezeichnungen bei Wasser:
-
Nassdampf
- t = 100 °C, x < 1
- Gemisch aus Wasser und Wasserdampf
-
Sattdampf oder trockengesättigter Dampf
- t = 100 °C, x = 1
- gerade kein Wasser mehr im Dampf
-
Heißdampf oder überhitzter Dampf
- t > 100 °C, x = 1
- reiner Wasserdampf
-
Spezifische Verdampfungsenthalpie oder
Verdampfungswärme r:
- erforderliche Energie, um 1 kg bei konstantem Druck
zu verdampfen
- hängt vom Druck und vom Stoff ab
- ist 0 oberhalb einer bestimmten Temperatur
- für Wasser bei Normdruck r = 2256.5 kJ/kg
- Schmelzen:
- Übergang von der festen in die flüssige Phase
- Schmelztemperatur hängt nur schwach vom Druck
ab
- bei Schmelztemperatur Koexistenz von flüssiger und
fester Phase
- spezifische
Schmelzenthalpie oder Schmelzwärme
σ
- für Wasser bei Normdruck σ = 333.5 kJ/kg
- Sublimieren:
- direkter Übergang von der festen in die gasförmige
Phase bei sehr niedrigem Druck
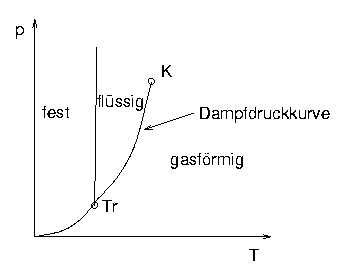
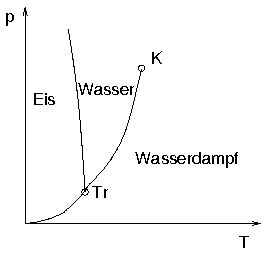
- Darstellung im p-T-Diagramm:
- typisches Verhalten
- Dampfdruckkurve p(T):
Druckabhängigkeit des Siedepunkts
-
Tripelpunkt
- Koexistenz aller drei Phasen
- bei Wasser pTr = 6.117 mbar,
TTr = 0.01 °C
-
Kritischer Punkt
- Druck pk und Temperatur
Tk, ab der r = 0
- darüber stetiger Übergang von Flüssigkeit zu
Gas
- bei Wasser pk = 220.64 bar,
Tk = 373.95 °C
- Anomalie des Wassers:
- spezifisches Volumen von Eis größer als von Wasser
bei 0 °C
- Schmelztemperatur sinkt mit steigendem Druck
- hartnäckiger
Mythos: ermöglicht Schlittschuhlaufen
- Ursache:
- Eis formt Kristalle mit großen Zwischenräumen
→ niedrige Dichte
- Wasser nahe 0 °C beginnt schon, sich zu
Eisstrukturen zu ordnen → Dichte sinkt
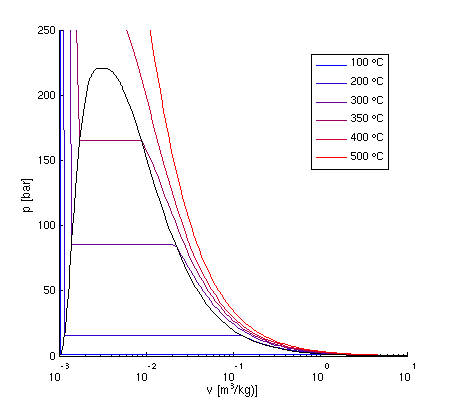
- Darstellung im p-V-Diagramm:
- exemplarisch für Wasserdampf
- Isothermen
- T groß → ungefähr Hyperbeln
- im Nassdampfgebiet (Verdampfung): waagerechte
Abschnitte, also isobar
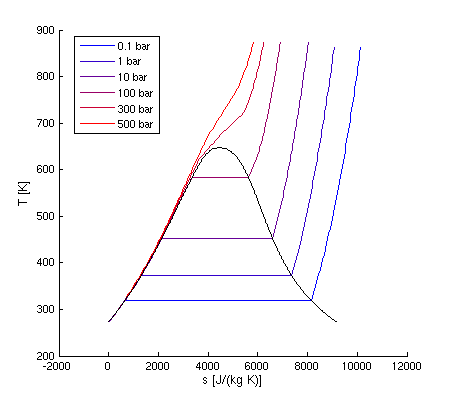
- Darstellung im T-S-Diagramm:
- exemplarisch für Wasserdampf
- Isobaren
- T groß → Verlauf wie beim idealen Gas
- im Nassdampfgebiet: waagerechte Abschnitte, also
isotherm
- Aufgaben: